初の準男爵であり,人類最多の元素発見者であり,「最大の功績はマイケルファラデーを見出したこと」と言われ拗ねたハンフリー・デービーが,ボルタ電池による電気分解で発見した元素に「カリウム(K)」があります。
カリウム金属の製法のひとつとして,塩化カリウムのナトリウム還元による熱的製法があります。
KCl + Na > NaCl + K
ナトリウムは,0価から+1価に酸化されていますので還元剤として働いています。つまり,ナトリウムの方がカリウムに比べて酸化されやすい(電子を出しやすい)ことが想像できます。
一方で,イオン化傾向(Li, K, Ca, Na, Mg, Al, Zn, Fe, Ni, Sn, Pb, H2, Cu, Hg, Ag, Pt, Au)を眺めますと,ナトリウム(Na)とカリウム(K)とではカリウムの方が酸化されやすい(電子を出しやすい)ことがわかり,先ほどの結果と逆の結論になります。
また,標準電極電位からも、(当然)カリウムの方が酸化されやすい(電子を出しやすい)ことがわかります。
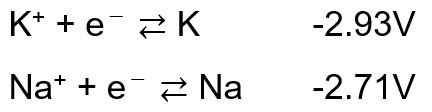
つまりは,塩化カリウムはナトリウムにより還元されないはずなのですが,実際には還元されカリウム金属の製法あるいはナトリウムカリウム合金の製法として知られています。
この通常起きえない反応が起きる理由(だから,問題になりやすいのです)は,塩化ナトリウム(NaCl;785.53kJ/mol)の方が塩化カリウム(KCl ;716.76kJ/mol )に比べて格子エネルギーが大きく,酸化還元エネルギーの不利をうわまわるために,反応が進行します。
【参考文献: 格子エネルギー;D.D. Wagman, W.H. Evans, V.B. Parker, R.H. Schumm, I. Halow, S.M. Bailey, K.L. Churney, R.I. Nuttal, K.L. Churney and R.I. Nuttal, The NBS tables of chemical thermodynamics properties, J. Phys. Chem. Ref. Data 11 Suppl. 2 (1982).】
ちなみに、おススメの岩塩はコチラです。

授業中の「ネタ話」等々を,このぐらいの文量で書いていきます。





![[YouTube動画]電子軌道と電子配置と周期表の成立ち](https://tomonolab.com/wp-content/uploads/2021/11/6034-000855-56a12ee85f9b58b7d0bcd9f8-5c759a244cedfd0001de0ad9-150x150.jpg)






[…] >> カリウム(K)の製法は,塩化カリウムのナトリウムによる還元が可能な理由 […]