さて,2022年の高等学校1年生から新学習指導要領が始まっています。Twitterなどで,時折話題に上りますので,先生垢や受験生垢はどこかでご覧になっているかと思います。
改定の基本的な考え方
さて,2022年度の改定の基本的な考え方として,いくつかあるんでしょうが下記2点に注目しています。
- 「学力の3要素」の枠組みや内容を維持したうえでの,知識の理解の【質】の向上と確かな学力を育成すること。
- 高大接続改革を念頭に,高等学校で学ぶ内容と大学で学ぶ内容がスムーズに移行できるようにする。
①については,「暗記」ではなく,「知識」をどう使うかを学ぶことかと思います。
②については,「熱化学方程式」を代表とする【日本の高校生だけが学ぶ単元】をなくし,日本の大学での教育および,当然のことながら海外の大学進学も視野に入れたグローバルに通用する教育かと思います。>> 熱化学方程式の問題点のブログはコチラ,YouTube動画はコチラ

さて,高校化学への理論的内容の追加は,「暗記が減る」ので私としては大歓迎です。
一方で,「用語」変更は暗記です。改訂ごとに「ぱっと見」でまとめておきます。
ということで,変更となった用語をまとめておきます。
- 旧課程で既に対応済みの用語も含みます。
- 教科書によっては,対応している場合としていない場合があります。
※時間を見つけて,理論化学・有機化学・無機化学の単元毎にまとめていこうかと思います。
変更された用語一覧
理論化学
物質の表記方法・表現方法
イオン式 → イオンを表す化学式(Ionic formula)
Na+やCl-は,イオン式と言われてきたが「イオンを表す化学式」あるいは「化学式」と改訂されました。また,「イオン反応式」も重要語句(太字)の扱いがなくなりました。
絶対質量 → 質量(mass)
物質の質量には,相対質量と絶対質量がありました。絶対質量とは「物質の質量そのもの」であり,相対質量とは「基準物質(12C)に対する質量」です。今回,絶対質量が「質量」となりました。
例えば,炭素の(絶対)質量は,1.9926×10^-23 g/mol です。水素の(絶対)質量は,1.6735×10^-24 g/molです。この値からも,とても小さい値で,また書くのが”若干めんどくさい”こともわかります。
ここで,炭素原子の質量/水素原子の質量 (;19.926×10^-24/(1.6735×10^-24) = 11.91) ≒ 12と算出されます。炭素原子の【相対】質量を「12」と置くことで,水素の相対質量は「1」となります。
このように,数値の大小を直感的にわかりやすく,表記しやすくしたのが「相対質量」です。
価標 → 用いない (bond)
化合物の化学構造を図字する際に,結合の事を「価標」と言います。単結合は1本線,二重結合は2本線,三重結合は3本線で表示します。これがなくなったわけです。そういえば,一度も使ったことのない言葉でした。。。
標準状態 → 用いない(0℃,1.013×10^5 Pa と明示)
これまで,標準状態()と暗黙に標準な状態を定義されてきましたが,改訂に伴い具体的な数字で明記されることになりました。こちらの方がわかりやすいし,標準状態の圧力(atmとPaとmmHg)などややこしかったので,良いかと思います。
希ガス → 貴ガス(Noble gas)
第18族元素の事です。英語表記も「Rare gas」でしたが,2005年以降は「noble gas」に変更されました。この英語表記変更に伴い,日本語も「希ガス」から「貴ガス」へ変更です。
最近の語呂合わせは,かっこええですね!思わず感激したので掲載しました。
「ヘリでネオン街に降り、歩いてクリップの奇跡よ起これ = ヘリ(ヘリウム、He)でネオン(ネオン、Ne)街に降り、歩(アルゴン、Ar)いてクリップ(クリプトン、Kr)の奇跡(キセノン、Xe)よ起これ」
結晶の名称
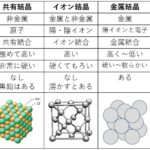
共有結晶 → 共有結合の結晶 or 共有結合結晶 (Covalent crystal)
共有結合による形成される結晶を「共有結晶」と一部で言われていました。私も,そのように学んでいました。
金属の結晶 → 金属結晶 (Metallic crystal)
金属結合によって形成される結晶を「金属結晶」と呼ぶ。教科書や参考書で「金属の結晶」と「金属結晶」が混在化していたので統一されました。
>> 【YouTube動画】電気陰性度で分類する化学結合と結晶 電気陰性度により,結合を分類しています。 結合には,イオン結合・共有結合・金属結合・分子間力があります。それぞれに対応した「結晶名」があります。
六方最密充填 → 六方最密構造
結晶構造の名称のひとつ。同時に学ぶ構造として,体心立方格子・面心立方格子があります。
昇華(気体→固体) → 凝華 (deposition, desublimation)
ヨウ素やドライアイス(CO2)のように固体から気体になることを昇華と言います。この固体から気体になる現象も「昇華」と言っていましたが,新課程では「凝華(ぎょうか)」と言います。
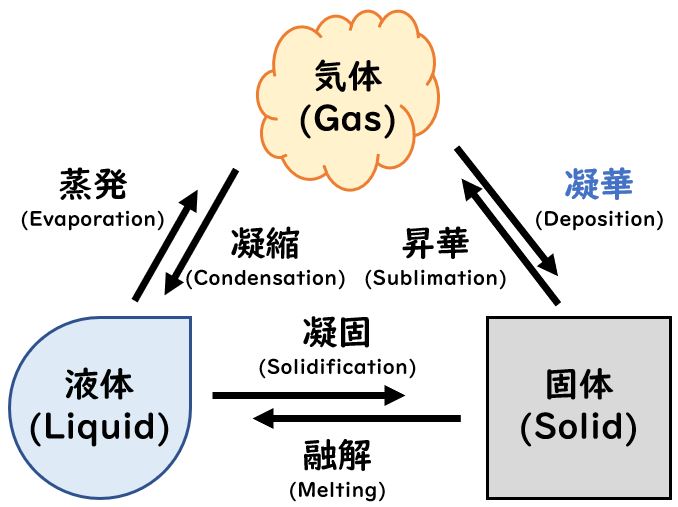
物質の三態
今回の気体から固体への変化が「凝華」となったことから,物質の運動状態が減少する方向には全て「凝(ぎょう)」という言葉が付くことになりました。
気体 → 液体 : 凝縮
液体 → 固体: 凝固
気体 → 気体: 凝華
アルカリ土類金属 (2族全て)
これまで,Be,Mgをのぞく金属をアルカリ土類金属と呼んでいました。これが変更になります。なぜ,ベリリウムとマグネシウムが「アルカリ土類金属」から除かれていたかというと,他のアルカリ土類元素と異なり,ベリリウムとマグネシウムは「水と反応しない」と「炎色反応を示さない(白色色)」という特徴があります。
>> 詳しくはコチラを参照してください。
遷移元素 (12族元素も含む)
12族の亜鉛(Zn),カドミウム(Cd),水銀(Hg)が遷移元素(Transition element)になりました。この変更については,金属錯体を扱ってきた研究者として「少し違和感」があります。
>> 軽くはコチラを参照してください。
>> 原子軌道も含めた詳しいのはコチラを参照してください。
沸点上昇度(凝固点降下度) → 沸点上昇(凝固点降下)
表現の統一ですね。
>> 【YouTube動画】混合物の凝固点降下や沸点上昇がなぜ起きる? 沸点上昇と凝固点降下および浸透圧を ・エントロピー ・化学ポテンシャル の二つの方法で考察しています。
熱化学方程式 → エンタルピー (エントロピー)
高校化学と大学基礎化学の大きな弊害が取り除かれました。めでたい!
>> 文章での解説は 詳しくはコチラを参照してください。
活性化状態 → 遷移状態
工事中
法則名の変更と変更案
質量作用の法則 → 化学平衡の法則
化学反応に関係する物質の質量(濃度)が,その反応の平衡にどのように影響するかを示す法則の事です。化学反応は全てが完全に進行する訳ではなく,正反応と逆反応が釣りあうことで,一見反応が進行していないように見える状態があります。
この反応が進行していないように見える状態を「化学平衡」と言います。
化学平衡においては,どのようにすれば目的物質が多く生成される反応に偏るのかを考えます。この反応の偏りの際に「ルシャトリエの原理」が出てきます。
>>【YouTube授業動画】ファント・ホッフの式でルシャトリエも理解 「ゆっくり丁寧」 ルシャトリエの原理 ・濃度が変化した時 ・圧力が変化した時 ・温度が変化した時 ・触媒を加えたとき
今後変更される可能性のある法則名
定比例の法則 → 一定組成の法則
倍数比例の法則 → 倍数組成の法則
気体反応の法則 → 反応体積比の法則
有機化学?
アルデヒド基
工事中
ケトン基
工事中
光学異性体
工事中
アクリル系繊維 → モダクリル繊維
令和4年に家庭用品品質表示法に変更があり,それに合わせて変更される。
無機化学?
Fe(OH)3 → 化学式では表記しない
Fe(OH)3とこれまで書かれてきましたが,様々な鉄化合物の集合体です。そのため,化学式ではなく物質名で表記されることになりました。
>> 詳しくはコチラを参照してください。
融解塩電解 → 溶融塩電解
イオン化傾向が大きい金属(Li, K, Ca, Na, Mg, Alなど)のイオンは,水溶液中で還元されて単体が生成することはありません。これらの金属の単体は,それぞれの塩化物・酸化物・水酸化物などを高温で融解させて電気分解することで,陰極側で得ることができます。これを溶融塩電解という名称に統一します。
(※ 物質の三態として,融解を使っているので融解塩電解でもいいのですが,確かに通名は「溶融塩」のような気がするので,こちらに合わせたんですね。)
さて,カリウム(K)の製法として,塩化カリウムでナトリウム還元できます。これはナトリウムとカリウムのイオン化傾向(標準電極電位)がわかっていれば,逆反応が進みそうなものですが・・・
>> カリウム(K)の製法は,塩化カリウムのナトリウムによる還元が可能な理由
参考教科書およびサイト
おススメ参考書
「資質・能力」を育む高校化学 探究で変える授業実践 / 後藤顕一 【本】
下記、参考書は毎年出版されているものです。【旧課程】を間違って購入しませんようお気を付けください。
第一学習社
>> 教科書がPDFで閲覧できます。
実教出版
>> 教科書がPDFで閲覧できます。
日本化学会
上記,改訂の用語は,ほとんどが「日本化学会」の提案を基に実施されているかと思います。日本化学会とは言わずも知れた「日本の中で最大の化学系の学会」です。
> 【お知らせ】高等学校化学で用いる用語に関する提案(1)への反応
▼
これらを参考に記載しておりますが,修正が必要な場合はコメントいただけますと幸いです。
















[…] 新課程での用語や定義の変更一覧を紹介しています。 > コチラ […]
質量作用の法則 → 化学平衡の法則
「law of mass action」を誤訳(直訳)して「質量(mass)作用(action)の法則」としていたものです。
この法則は,質量とは全く関係がありません。
「mass action」で「化学平衡」と訳すべきだったものです。
同様に,「電子親和力」も「エネルギー」であるにもかかわらず「力」と誤訳されたままになっています。
いずれ訂正されるものと思っています。
コメントありがとうございます。留学生さんを相手にすると母国語で学ぶことができることの有利さが身にしてみて感じます。東南アジアの国では,サイエンスを母国語で学べずに英語で学びます。英語で学べるからいいじゃないか!という意見もありますが,やっぱり母国語特有のニュアンスまではわかりません。日本で優秀な科学者が育つ理由も日本語と言う母国語でサイエンスを学べるからかもしれませんね。そういった意味では,多少の誤訳も味わい深く感じます。
[…] 新課程で変更となった化学基礎・化学の用語もまとめています > こちらをクリック […]